李东1,2,王忠铭1,2,袁振宏1,吴创之1,廖翠萍1
1中国科学院广州能源研究所,广州,(510640)
2中国科学院研究生院,北京,(100039)
摘要:七十年代以来,开发低成本、可持续和可再生能源已成为各国的研究热点。以生物质为原料生产的燃料乙醇是一种很有应用潜力的能源。本文简要讨论了生物质合成气发酵生产乙醇的技术途径,分析了该技术的优点、工艺过程、生产成本和市场化进程,特别介绍了美国BRI公司和密西西比乙醇公司(ME)在生物质合成气发酵生产乙醇方面所做的工作;同时,指出了对我国发展生物质合成气发酵技术的必要性和应用前景。
1.引言
能源是现代社会赖以生存和发展的基础,液体燃料的供给能力与国民经济可持续发展密切相关,是国家战略安全保障的基础之一。液体燃料的不足已严重威胁到我国的能源与经济安全,为此我国提出了大力开发新能源和可再生能源、优化能源结构的战略发展规划[1,2]。生物质是惟一可以转化为液体燃料的可再生能源,将生物质转化为液体燃料不仅能够弥补化石燃料的不足,而且有助于保护生态环境。生物质包括各种速生的能源植物、农业废弃物、林业废弃物、水生植物以及各种有机垃圾等。我国生物质资源丰富,理论年产量为50亿吨左右,发展生物质液化替代化石燃料有巨大的资源潜力[3]。
乙醇是一种优质的液体燃料,每千克乙醇完全燃烧时约能放出30000kJ的热量。乙醇燃料具有很多优点,它是一种不含硫及灰分的清洁能源,可以单独作为燃料使用;同时,一定量燃料乙醇加入汽油后,混合燃料的含氧量增加,辛烷值提高,降低了汽车尾气中有害气体的排放量。事实上,纯乙醇或与汽油混合物作为车用燃料,最易工业化,并与先进工业应用及交通设施接轨,是最具发展潜力的石油替代燃料[4]。
乙醇的生产方法可概况为两大类:发酵法和化学合成法。化学合成法是用石油裂解产出乙烯气体来合成乙醇,有乙烯直接水合法,硫酸吸附法和乙炔法等,其中乙烯直接水合法应用比较多。目前,乙醇生产主要是糖质作物(甜菜,甘蔗等)和淀粉质作物(玉米,土豆等)的直接发酵,以及纤维质原料(玉米秆,稻草等)的水解-发酵这两种工艺。
在人们探索生物质液体燃料生产技术过程中,生物质合成气发酵生产乙醇无疑是一种新方法,它是一种由生物质间接制备乙醇的方法,集成了热化学和生物发酵两种工艺过程。首先,通过气化反应装置把生物质转化成富含CO,CO2和H2的中间气体,这些气体被称作生物质合成气,然后,再利用微生物发酵技术将其转化为乙醇。
2.生物质合成气乙醇发酵工艺的优势
从使用的原料角度来看,化学合成法显然不适宜,石油是不可再生资源,它的利用违背了可持续发展和环保的原则,现在,发酵法生产的乙醇占全球总量的95%以上[5],其中绝大部分的燃料乙醇产业化生产都以粮食为生产原料,如巴西以甘蔗为原料,美国和欧盟国家则以玉米和小麦为原料,然而,占生物质资源70%以上的纤维素类原料也可以用于生产乙醇等液体燃料。
无论是直接发酵还是间接发酵都存在一些问题:这两种工艺的产业化都需要国家的财政补贴,高成本的水解酶以及废液的形成(含有酸预处理和生物质酸水解过程中产生的有毒化合物);另一方面,当利用生物质时,大约10~40wt%的木质素不能被降解成可发酵化合物。为克服上述问题,已经有很多科研工作者进行了大量的努力工作[6],但效果不是很好。
这里介绍的生物质合成气发酵制乙醇工艺过程,它将全部生物质(包括木质素以及难降解部分)通过流化床气化过程转化成合成气,既提高了生物质的利用率,也解决了木质素废液的处理问题。
合成气也可以通过化学催化转化(F-T合成)成液体燃料[7],但与合成气的乙醇发酵工艺相比,后者更具吸引力:(1)化学催化需要高温高压条件,这导致热效率损失和较高的加热成本,然而,微生物的发酵转化是在低温低压条件下完成,这样可以降低能量和设备成本,增强了生产安全性;(2)微生物转化与化学催化相比可以提高产率,因为只需很少一部分底物用于微生物生长;(3)在适宜条件下,微生物转化具有较高的选择性,可以转化成一种主要产品;(4)生物催化剂-细胞的回收以及再生较为容易;(5)生物质合成气流量和气体组成比对反应过程影响不大;(6)发酵过程没有硫化物中毒的情况。
3.基本流程
3.1生物质气化
气化过程需要在一定的温度下进行,以免产生大量灰渣,还应该在氧不足的条件下气化,以免过分燃烧且合成气中含有O2(影响后面的发酵过程)。根据原料的不同操作温度有所不同,一般情况下反应温度在750-800℃,压力要求仅比大气压稍高。当温度上升到850℃,生物质中的碱金属可能会熔化粘结导致流化床中砂子的结块降低流化效率。在此条件下获得的合成气主要包括N2,CO,CO2,H2,CH4。俄克拉荷马州立大学的Datar等人[8]以柳枝稷为原料,操作温度为770℃,氧气和生物质进料质量比为0.33的条件下得到的典型合成气组分为50~60%N2,14~19%CO,15~18%CO2,3~5%H2,4~5%CH4。还有少量NOX,C2化合物以及焦油,这些成分不进入下一步的发酵反应。根据设计,这些成分可以进入气体整合设备,转换成生物质合成气;或者通过最后焚烧和发酵尾气混合成为气化炉的部分燃料。
3.2发酵过程
整合后的合成气进入发酵设备后通过细菌的作用转化成乙醇。生物反应器的类型,尺寸,培养基成分,菌种,合成气成分以及操作条件均会影响乙醇产率。
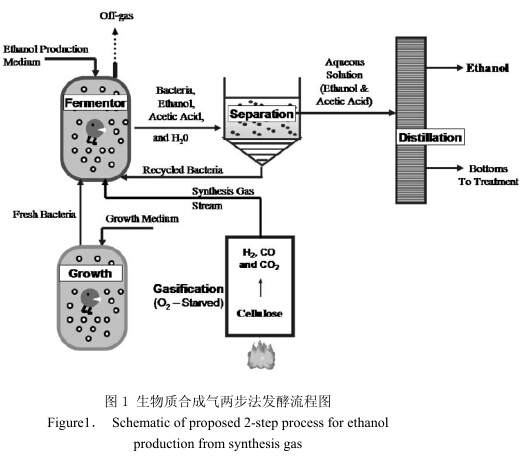
Gaddy和Clausen[9]通过实验发现,在间歇培养没有连续气体供给,由于传质效果很差,细胞对合成气的吸收依赖于气体的溶解度,只有3.5%的CO发生转化,pH5.0条件下,发酵液内乙醇浓度少于1g/l,乙醇和乙酸的摩尔比是0.05;间歇培养,培养基中没有酵母粉,连续气体供给,pH4.0时,经过320h反应后,乙醇浓度达到7g/l,乙醇和乙酸的摩尔比增加到9。采用两步连续操作搅拌槽式反应器(two-stageCSTR),成功地提高了乙醇产量和乙醇与乙酸地摩尔比。它将细胞生长和乙醇生成分开(因为合成气的乙醇发酵是产物生成非相关型),第一个反应器里是富含糖分细胞生长培养基,用于促进细胞生长,第二个反应器里是乙醇形成培养基,用于富集乙醇,见图1。
Klasson[10]Phillips[11]和Arora[12]等人分别对不同的菌株,不同的培养基,不同的合成气成分以及不用操作条件(气体流率,液体流率,气相停留时间,液相停留时间,液体稀释率,搅拌速率等)下,乙醇发酵情况做了详细的实验研究,包括对细胞的出口浓度,乙酸和乙醇的出口浓度,乙酸和乙醇的比生成速率,CO和H2利用率和转化率,乙酸和乙醇得率的影响。
Phillips等人通过实验得出结论,传质过程在整个合成气乙醇发酵过程中是速率控制步骤,提高气体流率并不能够提高传质速率,因为气体在发酵液中的溶解度都很低,导致较低的乙醇产率。为了克服上述限制,Klasson等人[10]采用填充床鼓泡床反应器(packed-bed bubble columns)和滴流床反应器(trickle bed columns),前者采用逆流地操作方式,后者采用并流地操作方式,不幸的是在他们的文章中没有给出乙醇产率。为了进一步提高气液传质面积,提高产率,Bredwell和Worden等人[13]采用微泡床反应器使用O2模拟合成气的乙醇发酵过程。
发酵微生物菌体的循环使用对合成气的转化影响很大。1996年Arora[14]利用菌株BRIO-52得到如下结果:
菌体全部循环使用GRT=16.6min,LRT=31hr乙醇浓度=21g/l
27%的菌种更新GRT=7min,LRT=17hr乙醇浓度=22.3g/l
35%的菌种更新GRT=5.85min,LRT=12hr乙醇浓度=19.4g/l
其中:GRT为气体停留时间;LRT为发酵液停留时间
整个发酵过程CO转化率>80%,H2转化率为50-60%。他在两步CSTR实验过程中,保证每个过程中气体停留时间和液体停留时间一样。气体停留时间9分钟,乙醇浓度会达到30g/l,CO转化率为87%,H2转化率62%,乙醇的产量可以达到理论值的90%。
密西西比大学[15]对乙醇生产过程进行了优化,对各种发酵方法建立了相应的理论模型,包括基于藻酸盐的固定化细胞发酵和两步法发酵系统。
3.3分离提纯
发酵过程结束后,通过膜分离系统将细菌回收再利用;实际上,含有乙醇的发酵液通过三个不同的过程最终得到无水乙醇:首先通过蒸发系统得到浓度为7%的乙醇溶液,进一步通过精馏系统达到乙醇的共沸浓度,最后通过分子筛脱水得到无水乙醇[16]。
4.关键技术现状
4.1气化方法的选择
为了提高该技术的经济竞争力,应该选择较适合的气化炉并对其优化,以得到尽可能多的CO和H2,减少C和H以CO2和H2O的方式流失。俄克拉荷马州立大学对柳枝稷和百慕大群岛草通过三种反应器操作方式进行气化:空气气化,高温裂解和蒸汽裂解气化。对于柳枝稷,通
过上述三种方法气化,平均CO浓度从20%提高到47%,平均H2浓度从6%提高到18%;而对于百慕大群岛草,平均CO浓度从16%提高到34%,H2浓度从6%提高到28%。从上面的数据可以看出,采用蒸汽裂解气化对于提高乙醇产量更具有优势。
4.2发酵菌株
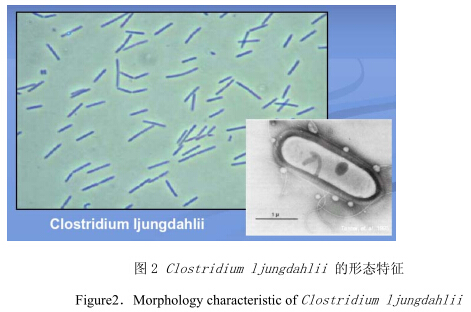
80年代末,美国阿肯色州立大学的Gaddy博士[9]和他的助手就开始了生物质合成气的发酵研究。他们从家禽的生活垃圾(鸡粪)中分离到能够利用合成气生成乙醇和乙酸的一株纯培养物,并对其进行形态学和生物化学特性鉴定,证明它是一种新的厌氧梭菌,命名为Clostridium ljungdahlii,1992年对该菌株拥有专利保护(ATCC49587)。它的形貌特征见图2,微生物学特性为:呈棒状,具有运动性;很少形成芽孢;严格厌氧,革兰氏阳性细菌;最适生长温度37ºC;最适生长pH5.0~7.0,此时主要的合成气发酵产物为乙酸,在37ºCpH4.0-pH4.5时,主要产物为乙醇。
90年代,俄克拉荷马州立大学的Tanner等人[17]也从农业泻湖里分离得到P7,能够利用合成气生成乙醇和乙酸,经过16SrRNA寡核苷酸编目分析和核酸分子(DNA-DNA)杂交分析鉴定,均证实它是一种新梭菌。P7的重要特点包括极好的菌种稳定性,对氧有一定的耐受性,对高浓度的乙醇也具有耐受性,而且在组合培养基里也有生长能力。
密西西比州立大学目前在美国能源部支持下也开展生物质合成气发酵生产乙醇的研究,Zappi博士和French博士是目前该大学从事这项工作的主要研究人员,该大学生命科学系的Brown博士分离得到一株嗜温菌(MSU1),经实验证实该菌具有合成气乙醇发酵能力。在他们的指导下,Morrison女士[18]于2004年采用两步CSTR法,对MUS1和Clostridium ljungdahlii的细胞生长,乙醇产生及其相应培养基做了比较工作。她同时也做了野生菌株筛选和培养驯化工作,虽然没有分离出新的菌株,但证明在马粪、沼气发酵罐内均存在能够转化CO为乙醇的微生物。
能够利用合成气的微生物都是厌氧菌,可分为自养菌和单碳自养菌[19]。自养菌利用C1化合物(CO和/或CO2)作为唯一碳源,氢作为能源;单碳自养菌利用C1化合物同时作为唯一碳源和能源。目前经过证实,具有合成气乙醇发酵能力的微生物有下面几种:Acetobacterium woodii,Butyribacterium methylotrophicum,Clostridium thermoaceticum,Clostridium ljungdahlii,Eubacterium limosum,Methanobacterium formicicum,Methanobrevibactersmithii,Methanosarcina barkeri,Methanospirillumhungate,Methanothrix soehngenii,Peptostreptococcus productus,Rhodopseudomonas gelatinosa,和Rhodospirillum rubrum.Arora等人[12]在1995年报导,分离物ER-12、ER-18、BRIO-52和BRIC-01也具有将生物质合成气转化为乙醇的能力。
4.3发酵菌株的代谢途径以及关键酶
合成气发酵产乙醇的微生物代谢途径已经有报道[20],厌氧细菌(例如Clostridium ljungdahlii和Clostridium autoethanogenum)利用CO,CO2,H2发酵产生乙醇和乙酸是通过产乙酸途径完成的,也就是厌氧乙酰-辅酶A(acetyl-CoA)途径。在发酵过程中,通常还伴有丁醇的生成。综合反应过程如下:
6CO+3H2O→CH33CH2OH+4CO2
2CO2+6H2→CH3CH2OH+3H2O
4CO+2H2O→CH3COOH+2CO2
2CO2+4H2→CH3COOH+2H2O
12CO+5H2O→C4H9OH+8CO2
12H2+4CO2→C4H9OH+7H2O
在乙醇形成过程中,主要包括三个酶:一氧化碳脱氢酶(CODH),甲酸脱氢酶(FDH)和氢化酶,其中,CODH是乙酰-辅酶A途径的关键酶。形成的乙酰-辅酶A,在生长条件下转化成细胞,乙酸和ATP,此时,乙酸为最终电子受体并产生大量ATP用于细胞生长;在非生长条件下转化成NADH和乙醇,此时,乙醇为最终电子受体并生成大量还原力NADH,少量的ATP只维持细胞功能,不用于细胞生长[21]。在37ºCpH5.0-pH7.0时,细胞处于生长阶段,主要产物为乙酸;pH4.0-pH4.5时,细胞处于非生长阶段,主要产物为乙醇,从这里可以看出,生物质合成气的乙醇发酵为产物生成非相关型。
4.4合成气成分对发酵的影响
和其它的合成气反应过程相比,合成气发酵过程并不需要严格的H2和CO的比例,菌体虽然偏好CO,但是CO和H2/CO混合物几乎同时被转化。
Lewis等人[22]通过比较实验得出结果,与“干净”的罐装气体(成分与合成气相似)相比,合成气会抑制细胞生长但是不会促使细胞死亡;另外,乙醇产率有明显提高。合成气经过丙酮清洗和0.025µm滤膜过滤后能够去除生长抑制剂,但是单独的净化过程均不能去除抑制
剂。在任何情况下,与“干净”的罐装气体相比,H2的利用率都有所降低,这可能是合成气中的NO和乙炔影响了氢化酶的活性从而抑制了H2的利用,进一步的工作将是确定合成气中的哪些痕量物质抑制氢的利用。
从旋风分离器出来的合成气中可能含有微量的O2,Datar等人[8]以P7作为发酵菌株进行发酵,经实验证明这一痕量的O2不会影响P7的生长和乙醇产量。
1995年,美国生物工程公司(BRI)[16]经过实验得出下列结论:在硫化物气体(H2S和COS等)含量2.5%的情况下对发酵有很小的的影响,达到5.2%时会延缓反应,超过10%时完全抑制细胞生长和CO的利用。对于一般的生物质合成气硫化物含量很小,整个反应过程的硫化物中毒现象很轻,完全可以避免。
而其它一些杂质(焦油等)对发酵过程影响的研究还没有结论。
5.成本分析与经济竞争性
1999年,Putsche等[23,24]建立了ASPEN模型,估算了在BCL/FERCO型气化炉内完成草根气化合成气制备和乙醇发酵的固定成本和运行费用。根据他的计算(依据美国当时的各项成本和补贴政策),一个月处理2,000吨干生物质原料的设备,每年将产166,800吨的乙醇,前提是每吨干生物质原料产258千克的乙醇。固定资本投资约为1.536亿美元,现金支出每千克乙醇0.191美元,原料成本每吨25美元。除去财政补贴和10%的税后折扣,得出的乙醇成本为每千克0.37美元。
Putsche的估算模型是基于现在的技术状况提出的,随着将来的技术进步,产率提高,固定资本投资降低等,这项技术将更具经济竞争力。
6.市场化进程
密西西比乙醇公司(ME)[16]在蒙塞拉特岛的威诺娜建成锯末气化装置。该设备最初设计是用来生产甲醇的,但是市场的变化使这个项目搁浅了。该公司和美国能源部签订了一份合同,评估用现存设备进行生物质气化发酵的可行性。其中Zappi博士提供了合同报告中合成气发酵技术的说明,并给予技术保障。评估报告结果如下:
发酵工艺以及设备能够和气化工艺相匹配。对进料量为30吨/天的干纤维质废料气化后,乙醇的产量将达到4000加仑/天。乙醇生产的这套设备成本大约为700-1000万美元。
对现有的气化装置需要一系列的改造,经过评估得出最小的改造成本大约是1,040,310美元。每年最少的运行费用和维护费用是180万美元。这些评估数据表明,只要乙醇的市场价格高于1美元/加仑,并且随着今后5到10年内投资成本的降低,收益将超过运行成本(到那个时候如果乙醇价格继续攀升的话,效益将更加明显)。因此,评估小组得出最后的结论:
通过ME工艺成功地生产乙醇是具有极大可能性的。
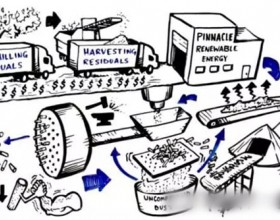
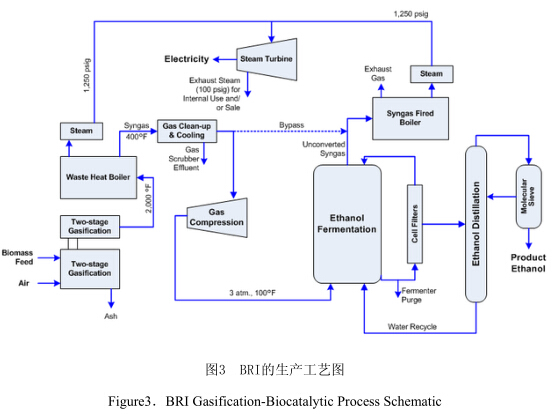
生物工程公司(BioEngineering Resources,Inc)[25]已经研发出合成气发酵技术,它能够成功地用纤维质垃圾高产快速地生产乙醇。该技术地工艺流程见图3。Gaddy博士负责公司的技术研发,开展这项研究多年,已经证明技术的可行性,目前正准备迈出商业化运作的第一步。需要耗费巨资处理的废弃物质经过气化后发酵,经济上可行,而且有利于环保。
BIR研制的生物反应器可以使发酵过程在常压下几分钟,增加压力一分钟的时间内完成,这样就使得反应成本大大降低。反应器内细菌的生长可以保证生物酶的更新。BRI已经对这一工艺过程申请了专利保护,包括细菌菌种,以及维持细菌良好的发酵环境的严格措施,因为微生物的发酵也有一些关键问题:营养物质,维生素,矿物质,毒素,污染源,以及pH的波动,BRI发酵过程的可靠性完全取决于是否能维持细菌的活性。
BRI在Gaddy博士领导下的小组对碳基物质进行气化和生物转化的研究,该项工艺可以完成气化发电和乙醇的联产。这些物质包括城市固体垃圾、生物质废弃物、废旧轮胎和塑料,还包括媒、天然气、精炼焦油和废油。BRI能够达到每吨干生物质产75加仑或是每吨废弃的轮胎或碳氢化合物产150加仑的乙醇。这个过程将使所有湿度低于30%的物质发生气化反应,包括废旧轮胎和塑料等转化为生物质合成气。热解气化在温度1200℃以上,在缺氧的条件下使有机物质裂解成为简单的CO,CO2和H2。合成气在通入发酵罐之前应该冷却到36℃,在这个过程会产生大量的热量,将这些热量用来产生高温蒸汽以驱动涡轮发电机发电。绝大部分原料,除了灰分和金属以外都可以转化成乙醇,因此产率将是非常高的,只有部分无机成分不能够转化,从气化炉里出来的无害剩余物可以作为垃圾填埋或是作会水泥预制块或铺路料等产品回收。
整个工程根据现在最大的气化炉设计,将建成分组的模块,容量可以根据需要进一步扩大。每一个模块包括两个气化装置,每一个装置可以日处理125吨生物质废弃物,同时配备两个发酵罐。每一个模块将年处理85000吨生物质,生产25480吨的乙醇,同时产生5MW电。
理论上,一个中等规模BRI可再生能源工厂能够每年处理1,000,000吨得MSW,废轮胎和(或)生物质固体废料,并产出80,000,000加仑的乙醇和50MW的电能,其中35MW是除去工厂本身所消耗后的净产量。这样一个工厂可能需要10个模块,占地面积大约30英亩。美国能源部给BRI提供240万美元示范这项技术。Gaddy在阿肯色州采用BRI工艺建立一个以生物质为原料的乙醇生产示范工厂,已经运行四年。这项技术已经具有商业应用价值,BRI的近期计划:
2005年末,建立第一个商业化运作装置;2006-2007年将陆续建立几个商业运行的装置。下面是正在商讨拟建的装置:
•德来斯波特(华盛顿),日处理300吨生物质
•兰开斯特(加利福尼亚),日处理250吨生物质
•阿曼(约旦),日处理1000吨生物质
•檀香山(夏威夷),日处理600吨生物质
7.我国发展这项技术的必要性及前景
生物质合成气发酵生产乙醇是一项颇具应用前景的实用技术,目前国际上专门从事这项研究工作的人很少,投入的资金也不多,美国一些相关人士正在积极呼吁加大投入,使这项技术能够快速发展起来。在俄克拉荷马州立大学,将低成本的生物质气化获得合成气,并进一步发酵制取燃料乙醇和其它化学品的研究作为一个主要方向,并组建了一个跨学科,跨机构的研究团队。为了得到在经济和环境上双赢的低成本,可再生能源,这项研究包括了一个从生物质生长到生产出乙醇的整体过程。具体包括:生物质原料的生产与运输;生物质气化生成合成气;合成气的发酵以及对整个过程的经济分析[26]。
我国正面临能源、环保两方面的压力,2005年2月28日通过了《中华人民共和国可再生能源法》。中国是一个能源消费大国,为了保证国家的能源安全,将更加鼓励可再生能源的研究,生物质合成气发酵生产乙醇技术将会在我国的可再生能源领域发挥重要的作用,将会得到国家的有力支持。
美国十几年的研究积累了一些成果,但仍然还存在一些技术和经济问题。首先是需要改进生物质的气化过程。选择气化装置增加CO和H2的产率对保障乙醇生产的经济运行十分重要。其次,虽然一些菌株证明可以将生物质合成气转化成为乙醇,但是还没有完全达到经济运行的目的,寻找一些潜在细菌,进行定向基因诱变以期达到更好的效果。再次,确定合成气中哪些物质(痕量气体和焦油)抑制氢的利用或是影响细胞生长和乙醇生产。最后,开发高气液传质速率的反应器,尤其重要的是,保证合成气发酵过程的稳定性和连续性。国内对这项技术的研究刚刚开始,还没有文章和报道,因此,我国科研人员可以介入这项研究同时也有必要对该新技术进行深入研究。
我国开展生物质合成气发酵合成乙醇的研究具有广泛的科研基础。国内生物质气化发电技术日臻成熟,在价格上同比国际市场很有竞争力。所以生物质气化发电不仅正在国内蓬勃发展,而且已经走出国门,向其它国家提供了技术服务。另外,国内在利用生物法将生物质原料合成液体燃料方面也积累了很多成功经验。这两方面的研究工作都为进行生物质合成气发酵生产乙醇做了充分的技术储备。
参考文献:
[1]阎长乐.中国能源发展报告2001 [M].北京:中国计量出版社,2001.15-35.
[2]倪维斗,靳晖,李政.[J].科技导报,2001,(12):9-12.
[3]袁振宏,李学凤,蔺国芬.我国生物质能技术产业化基础的研究[A].吴创之,袁振宏.2002 中国生物质能技术研讨会论文集[C].南京: 太阳能学会生物质能专业委员会,2002.1-18.
[4]袁振宏,吴创之,马隆龙等,生物质能利用原理与技术。北京:化学工业出版社 2005年3月.
[5]Davenport,R.E.,Gubler,R.,Yoneyama,M.,Chemical Economics Handbook Marketing Research Report-Ethyl Alcohol,SRI International,May 2002.
[6]Goncalves AR,Benar P.2001.Hydroxymethylation and oxidation of organosolv lignins and utilization of the products.Bioresource Technol 79:103–111.
[7]National Renewable Energy Laboratory.Gridley Ethanol Demonstration Project Utilizing Biomass Gasification Technology: Pilot Plant Gasifier and Syngas Conversion Testing.NREL/SR-510-37581,February 2005
[8]Datar RP,Shenkman RM,Cateni BG.2004,Fermentation of Biomass-Generated Producer Gas to Ethanol,www.interscience.wiley.com
[9]Gaddy J L,Clausen E C.“Clostridium ljungdahlii,an anaerobic ethanol and acetate producing microorganism.” US Patent 5,173,429.Dec.22,1992.
[10]Klasson,K.T.,C.M.D.Ackerson,E.C.Clausen,J.L.Gaddy.“Bioreactor Design for Synthesis Gas Fermentations.” Fuel.Vol.70,No 9,pp 605-614,1991.
[11]Phillips,J.R.,Klasson,K.T.,Clausen,E.C,and Gaddy,J.L.1993.“Biological Production of Ethanol from Coal Synthesis Gas – Medium Development Studies”,Appl.Biochem.Biotechnol.,39/40:559-571.
[12]Arora,D.,Basu,R.,Phillips,J.R.,Wilkstrom,C.V.,Clausen,E.C.,and Gaddy,J.L.1995.“Production of Ethanol from Refinery Waste Gases.Phase II.Technology Development”.DOE/AL/98770-1 (DE97006845).
[13]Bredwell,M.D.,M.Worden.“Mass Transfer Properties of Microbubbles.Experimental Studies.”Biotechnology Progress.Vol.14,No 1,pp 31-38,1998.
[14]Arora,D.,Basu,R.,Breshears,F.S.,Gaines,L.D.,Hays,K.S.,Phillips,J.R.,Wilkstrom,C.V.,Clausen,E.C.,and Gaddy,J.L.1996.“Production of Ethanol from Refinery Waste Gases.Final Report,April 1994–July 1997”.DOE/AL/98770-3 (DE98003194).
[15]Mark E.Zappi,W.Todd French,Christine E.Morrison,Katherine Taconi,Emily R.Easterling.“Isolation and Performance Optimization of Cultures Capable of Converting Syngas to Ethanol”.25th Symposium on Biotechnology for Fuels and Chemicals: Session 2
[16]Mississippi Ethanol LLC,“Final Report from Mississippi Ethanol LLC to the National Renewable Energy Laboratory”,NREL/SR-510-31720,March 2002.
[17]Rajagopalan S,Datar R P,Lewis RS.2002.Formation of ethanol from carbon monoxide via a microbial catalyst.Biomass Bioenergy 23:487–493.
[18]Christine Evon Morrison.2004.Production of Ethanol From the Fermentation of Synthesis Gas.UMI Number: 1421970
[19]Grethlein,A.J.and Jain,M.K.1992.“Bioprocessing of Coal-Derived Synthesis Gases by Anaerobic Bacteria”,TIBTECH,10:418-423.
[20]Rogers,P.1986.“Genetics and Biochemistry of Clostridium Relevant to Development of Fermentation Processes”,Adv.Appl.Microbiol.,31:1-60.
[21]Klasson,K.T.,M.D.Ackerson,E.C.Clausen.“Bioconversion of synthesis gas into liquid or gaseous fuels.”Enzyme Microbiology Technology.Vol.14,pp 602-608,1992b.
[22]Randy S Lewis,Asma Ahmed.“ETHANOL FROM BIOMASS: EFFECTS OF BIOMASS-GENERATED PRODUCER GAS”.www.aiche.org/conferences
[23]Putsche V,“Complete Process and Economic Model of Syngas Fermentation to Ethanol”,C Milestone Completion Report,National Renewable Energy Laboratory,August 31,1999.
[24]Spath P L,Dayton D C.2003.“Preliminary Screening —Technical and Economic Assessment of Synthesis Gas to Fuels and Chemicals with Emphasis on the Potential for Biomass-Derived Syngas”.NREL/TP-510-34929
[25]BRI Energy,Inc.The Co-Production of Ethanol and Electricity From Carbon-based Wastes.www.brienergy.com
[26]Oklahoma State University.September 28,2000.“Pilot System: Biogas to Ethanol & Feedstock Analysis”.www.westbioenergy.org